引言:十年来,从基础到临床,多发性骨髓瘤(MM)都有了大踏步前进。从国内少数单位可以诊断到大多数三级医院均可诊断;从大剂量美法仑以及ASCT的应用使患者生存期稍有延长到沙利度胺、硼替佐米等非细胞毒作用的高活性抗骨髓瘤药物使其治疗效果得到明显改善;以及第二代IMID来那度胺和第二代PI卡非佐米被批准用于MM的治疗,且最近又有抗CD38和抗CS1单抗以及HDACi帕比司他相继问世。MM治疗的CR率也从原来的5%左右提高到60%-70%,中位OS也达到6-7年。
新药造福患者
多项研究显示蛋白酶抑制剂/免疫调节剂联合/不联合明显提高诱导后和移植后完全缓解率(CR)和非常好的部分缓解率(VGPR),特别对于ISS Ⅲ期的高危患者能明显延长生存期。我中心1998.01-2015.05接受诱导治疗序贯自体外周血造血干细胞移植(APBSCT)的患者,接受硼替佐米/沙利度胺(123例)与不含硼替佐米/沙利度胺(21例)的中位PFS期分别为31.67个月和15.2个月,中位OS期为76.3个月和52.03个月。
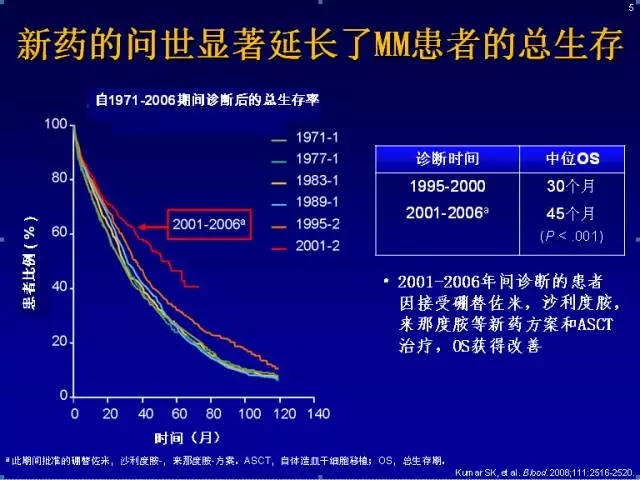
2008年Blood发表的一项研究显示:2001-2006年间诊断的患者因接受硼替佐米、沙利度胺、来那度胺等新药方案和ASCT治疗,较1995-2001年间未接受此类药物治疗的患者总体生存率(OS)获得明显改善,OS从30个月提高到45个月。
治疗时机明显提前

第56届美国血液学年会(ASH)发布MM的治疗指征改变,从过去的CRAB症状前移至SLiM CRAB标准。2014年IMWG共识认为“超高危冒烟型骨髓瘤(SMM)”应该诊断为活动性MM,一旦确诊,这些患者应按照初始MM接受治疗。
疗效标准更新
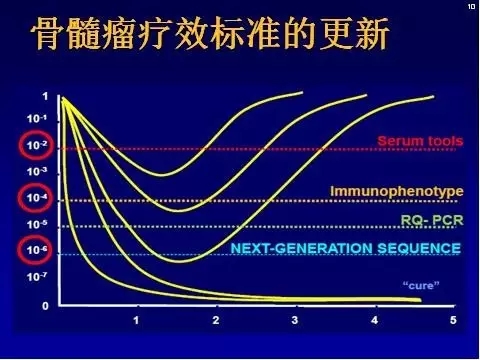
伴随着疗效的改善,人们追求MM治疗目标也越来越高,评估疗效标准越来越精确,过去常用血清学检测评估是否缓解,目前从免疫细胞分型、分子水平、二代测序、PET-CT等方面进行疗效评估,有助于临床早期判断疗效,制定个体化方案。
迈向MM的治愈之路
尽管近年来在MM治疗领域取得巨大进展,但MM整体上依然是一种不可治愈的疾病,绝大多数患者终将复发而不治,我们仍需向着治愈的目标前进。因此围绕MM的生物学特性,人们在基因、蛋白、代谢等多个层次,采用组学、基因编辑、新一代测序等新技术开展了卓有成效的工作,设计出对骨髓瘤表面分子、与微环境相互作用、胞内信号转导途径、肿瘤免疫的新型治疗策略,研发新的药物和新的治疗方法,为个体化治疗和精准治疗提供方向。
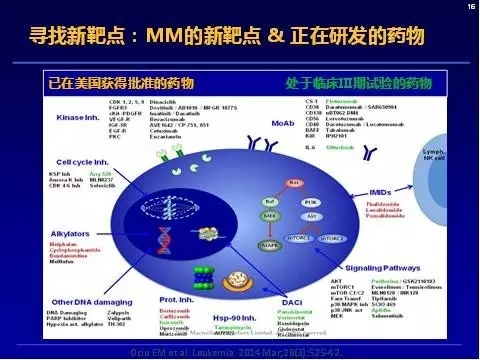
上图显示已在美国获得批准的药物有:激酶抑制剂、细胞周期抑制剂、其他DNA损伤药物等。处于临床Ⅲ期试验的药物有:Mo抗体,与信号通路有关的药物,组蛋白去乙酰化酶抑制剂、热休克蛋白抑制剂等。
Daratumumab是第一个被批准用于治疗多发性骨髓瘤的单克隆抗体,它是一种IgG1k抗体,人源化抗CD38单克隆抗体,具有广谱杀伤活性,靶向结合多发性骨髓瘤细胞表面高度表达的跨膜胞外酶CD38分子,可通过免疫耐受、免疫调节、直接抗肿瘤效应等多种机制诱导肿瘤细胞的快速死亡。多项研究显示单药或多药治疗MM效果良好。
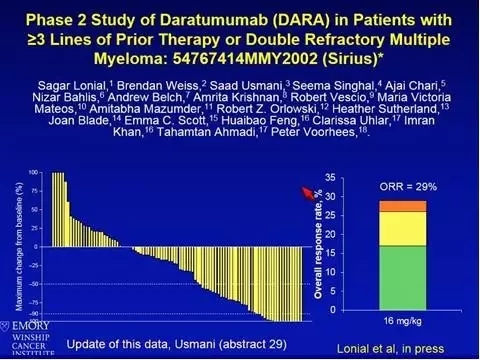
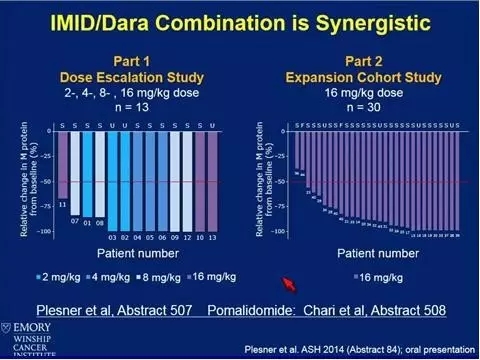
该研究显示DARA16mg/Kg应用在初治大于3期或复发难治的患者中,总体缓解率达29%。
Plesner等人的一项剂量递增和扩展队列研究均显示IMID联合DARA有协同作用。
继上述新药的不断开发,细胞免疫治疗也是目前肿瘤治疗的新途径,大多数嵌合抗原受体(CAR)通过识别肿瘤相关抗原scFv和胞内信号域在体外进行基因重组,生成重组质粒,再在体外通过转染技术转染到患者的T细胞,即嵌合抗原受体T细胞(CAR-T细胞)。CAR-T细胞在体内、外都具有对特定肿瘤抗原高度亲和性及对抗原负载细胞高效杀伤特性。近年来,不同靶点的CAR技术在MM体内及体外实验中获得较好的疗效。
启示
回顾十年来MM的进展,新药的诞生在骨髓瘤治疗方面取得良好疗效,从作用机制方面也提示我们攻克骨髓瘤需把握阴阳之道。骨髓瘤之阴在于浆细胞共有的生物学特性:如细胞存活因子、细胞膜连接蛋白等;骨髓瘤之阳在于瘤细胞特有的生物学特性:如免疫球蛋白转录家族、细胞遗传学异常、基因突变等。如蛋白酶体对蛋白的过度清除是许多肿瘤的发病机制之一,但只有在MM中PI才显现了明显的抗肿瘤作用。是因为PI既抑制了肿瘤发生的NF-ΚB途径,又通过抑制浆细胞共享的26S蛋白酶体,使未折叠蛋白不能降解,从而滞留于胞浆,触发骨髓瘤的凋亡。另外,IMIDs能和CRL4A泛素连接酶的一个接头蛋白CRBN结合,从而激活CRL4ACRBN泛素连接酶的活性来靶向并泛素化降解B细胞特异性的两个转录因子IKZF1和IKZF3,使得蛋白酶体降解,而IKZF1和IKZF3对B细胞的发育分化至关重要, IMIDs还能下调IRF4调节因子及MYC基因的表达,促进骨髓瘤细胞凋亡。
总之,十年来MM的治疗取得巨大进展,但仍不能治愈。未来的策略应兼顾其阴阳之道。
专家简介

侯健,长征医院血液内科主任、教授、博士生导师。从事血液系统基础与临床研究二十多年,主攻以多发性骨髓瘤为代表的浆细胞病,对该病的诊断、鉴别诊断、治疗方案的制定有较深的造诣。曾发表论文200余篇,有关工作曾获得上海市科技进步一等奖、中华医学科技二等奖等。兼任国际骨髓瘤工作组(IMWG)委员、中国抗癌协会血液肿瘤专业委员会常委、 中华医学会血液学会常委、中国医师协会血液专业委员会常务委员、中国病理生理学分会实验血液学分会委员、中国免疫学会血液免疫分会常委、上海市医学会血液分会主委等。





 京公网安备 11010502033352号
京公网安备 11010502033352号